O argônio é o gás inerte mais comumente usado em caixas de luvas e linhas Schlenk para experimentos altamente sensíveis. Embora o nitrogênio seja uma alternativa menos cara e mais frequente, o argônio é estritamente preferido quando há qualquer risco de o gás "inerte" reagir com os materiais experimentais, o que pode ocorrer com certos metais ou em altas temperaturas.
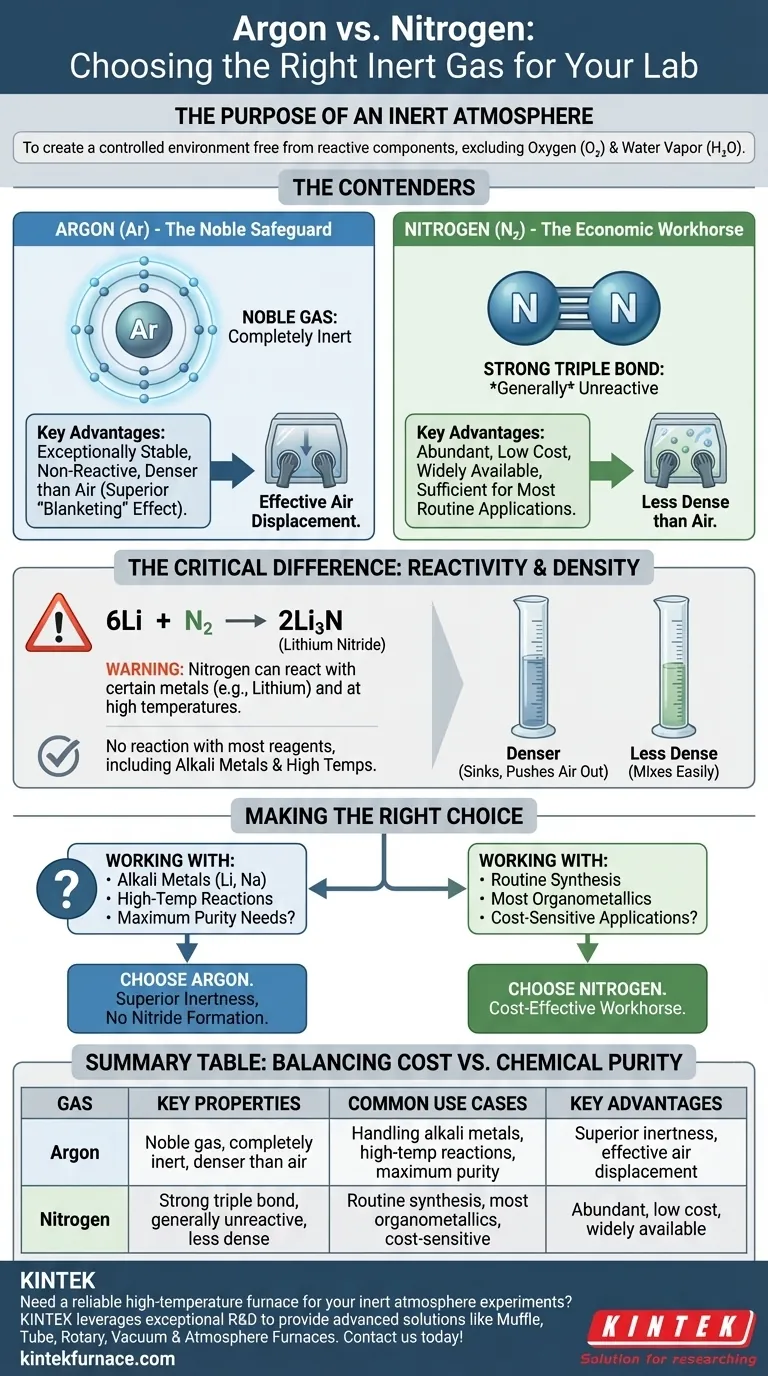
A escolha entre argônio e nitrogênio é uma decisão crítica na química sensível ao ar, equilibrando custo e pureza química. Embora o nitrogênio seja um cavalo de batalha econômico, o argônio oferece um nível superior de inércia, servindo como seguro essencial para experimentos altamente reativos ou de alta temperatura.

O Propósito de uma Atmosfera Inerte
A função principal de uma caixa de luvas ou linha Schlenk é criar um ambiente controlado livre de componentes atmosféricos reativos. Os principais culpados que você está tentando excluir são o oxigênio (O₂) e o vapor de água (H₂O), que podem decompor prontamente reagentes e catalisadores sensíveis.
Um gás inerte, como argônio ou nitrogênio, é usado para deslocar o ar e manter uma pressão positiva, evitando que qualquer vazamento atmosférico entre no sistema.
Comparando os Concorrentes: Argônio vs. Nitrogênio
Embora ambos sejam usados para criar uma atmosfera inerte, suas propriedades químicas e físicas determinam quando um é uma escolha melhor que o outro.
Nitrogênio: O Cavalo de Batalha Econômico
O nitrogênio (N₂) constitui cerca de 78% do ar que respiramos e, portanto, é abundante e barato.
A molécula de N₂ é caracterizada por uma ligação tripla muito forte entre seus dois átomos de nitrogênio. Essa ligação requer uma quantidade significativa de energia para ser quebrada, razão pela qual o nitrogênio é geralmente não reativo e adequado para uma ampla gama de aplicações químicas.
Argônio: O Protetor Nobre
O argônio (Ar) é um gás nobre. Isso significa que seus átomos têm uma camada eletrônica externa completamente preenchida, tornando-o excepcionalmente estável e não reativo.
Sob praticamente todas as condições de laboratório, o argônio não formará ligações químicas nem reagirá com seus reagentes. Essa inércia química fundamental é sua maior força.
A Diferença Crítica: Reatividade
O termo "inerte" é relativo. Embora o nitrogênio seja em grande parte não reativo, ele não é completamente inerte.
Sob condições específicas, o nitrogênio pode reagir com certos metais para formar nitretos metálicos. O exemplo mais comum na química sintética envolve o lítio metálico, que reage prontamente com o gás N₂ mesmo à temperatura ambiente para formar nitreto de lítio (Li₃N).
6Li + N₂ → 2Li₃N
Essa reação colateral indesejada pode consumir seu reagente e introduzir impurezas. Reações semelhantes podem ocorrer com outros metais alcalinos, metais alcalino-terrosos ou durante sínteses conduzidas em altas temperaturas. O argônio, como gás nobre, não tem essa desvantagem.
Uma Consideração Prática: Densidade do Gás
Uma diferença física fundamental é a densidade. O argônio é cerca de 40% mais denso que o ar, enquanto o nitrogênio é ligeiramente menos denso que o ar.
Isso significa que o argônio é mais eficaz em deslocar o ar de um recipiente, pois ele "afunda" e empurra o ar mais leve para cima e para fora. Esse efeito de "cobertura" o torna superior para purgar vidrarias em uma linha Schlenk e manter uma atmosfera estável dentro de uma caixa de luvas, pois ele se deposita no fundo em vez de se misturar facilmente.
Compreendendo as Trocas
A escolha do gás correto requer equilibrar a segurança absoluta com restrições práticas.
Custo: O Principal Impulsionador
A vantagem mais significativa do nitrogênio é o seu baixo custo. O argônio é substancialmente mais caro que o nitrogênio.
Para laboratórios que operam muitas caixas de luvas ou realizam síntese em larga escala, essa diferença de custo pode ser um fator importante. Por essa razão, o nitrogênio é frequentemente a escolha padrão para qualquer trabalho onde sua potencial reatividade não seja uma preocupação.
Pureza e Fornecimento
Ambos os gases estão comercialmente disponíveis em graus de pureza muito altos (por exemplo, 99,999%). A principal diferença muitas vezes reside no método de fornecimento.
Grandes usuários de nitrogênio podem ter geradores no local ou grandes vasos criogênicos de nitrogênio líquido que fornecem um suprimento contínuo de gás a partir da evaporação, reduzindo ainda mais seu custo operacional. O argônio é quase sempre fornecido em cilindros de gás de alta pressão, que exigem substituição regular.
Fazendo a Escolha Certa para o Seu Experimento
Sua decisão deve ser baseada na química específica que você está realizando.
- Se seu foco principal for síntese de rotina, purificação ou manuseio da maioria dos organometálicos: Use nitrogênio. Ele é suficientemente inerte para a grande maioria das aplicações e oferece economias de custo significativas.
- Se seu foco principal for trabalhar com lítio, outros metais alcalinos ou realizar reações de alta temperatura: Use argônio. Sua inércia superior é inegociável e protege seu experimento da formação de nitretos metálicos indesejados.
- Se seu foco principal for certeza máxima e eliminação de todas as variáveis: Use argônio. O custo mais alto é um pequeno preço a pagar pelo seguro de que seu gás inerte é verdadeiramente inerte.
Em última análise, compreender a reatividade sutil do nitrogênio é o que separa a prática de rotina do projeto experimental preciso e deliberado.
Tabela de Resumo:
| Gás | Propriedades Principais | Casos de Uso Comuns | Vantagens Chave |
|---|---|---|---|
| Argônio | Gás nobre, completamente inerte, mais denso que o ar | Manuseio de metais alcalinos, reações de alta temperatura, necessidades de pureza máxima | Inércia superior, deslocamento eficaz do ar, nenhuma formação de nitreto |
| Nitrogênio | Ligação tripla forte, geralmente não reativo, menos denso que o ar | Síntese de rotina, a maioria dos organometálicos, aplicações sensíveis ao custo | Abundante, baixo custo, amplamente disponível |
Precisa de um forno de alta temperatura confiável para seus experimentos em atmosfera inerte? A KINTEK alavanca P&D excepcional e fabricação interna para fornecer soluções avançadas como Fornos de Mufla, Tubo, Rotativos, a Vácuo e com Atmosfera, e Sistemas CVD/PECVD. Com fortes capacidades de personalização profunda, atendemos precisamente às suas necessidades experimentais únicas. Entre em contato conosco hoje para aumentar a eficiência e a segurança do seu laboratório!
Guia Visual
Produtos relacionados
- Forno tubular de quartzo para laboratório com várias zonas Forno tubular
- Forno de mufla de alta temperatura para desbobinagem e pré-sinterização em laboratório
- Forno de atmosfera controlada de correia de malha Forno de atmosfera inerte de azoto
- Forno de Mufla de 1200℃ para Laboratório
- Forno tubular rotativo com várias zonas de aquecimento divididas Forno tubular rotativo
As pessoas também perguntam
- Como funciona o sistema de controle de temperatura em um forno tubular experimental multi-gradiente? Domine Perfis de Calor Precisos para o seu Laboratório
- Que papel desempenham os fornos tubulares multizona na pesquisa de novas energias? Desbloqueie o Controle Térmico Preciso para a Inovação
- Por que os fornos tubulares multizona são particularmente úteis para a pesquisa de nanomateriais? Desbloqueie o Controle Térmico Preciso para Síntese Avançada
- Quais são as vantagens dos fornos tubulares multizona? Obtenha Controle Térmico Superior para Processamento Avançado de Materiais
- Como os fornos tubulares multizona são usados em pesquisa de cerâmica, metalurgia e vidro? Desbloqueie o Controle Térmico Preciso para Materiais Avançados



















